【化学——选修2:化学与技术】(15分)
通过海水能获得淡水、食盐、镁等,食盐可进一步用于氯碱工业。请回答下列问题。
(1)列举两种海水淡化的方法:_________、_________。
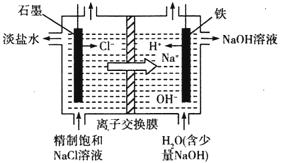
(2)氯碱工业通过电解饱和食盐水能获得烧碱和氯气等物质,该反应的化学方程式为_____________,如图是用离子交换膜法电解饱和食盐水的原理示意图。其中石墨接电源_________极,电解时铁电极的电极反应式为_________。电解过程中通过离子交换膜的主要离子是__________。
(3)侯氏制碱法中,首先向饱和食盐水中通入CO2和NH3制备NaHCO3,其化学方程式为____________;先通入的是__________(填化学式),其理由是__________________ ;再利用NaHCO3受热分解可制备纯碱。
(4)目前世界上60%以上的镁都是从海水中提取的,已知:MgO和MgCl2的熔点分别为2852℃和714℃。分析说明工业上采用电解熔融MgCl2而不是电解熔融MgO的理由__________ ______________________________________________________________________ 。
(1)蒸馏法、离子交换法、电渗析法(任选两个)(2分)
(2)2NaCl+2H2O电解2NaOH+H2↑+Cl2↑(2分) 正(1分) 2H++2e- H2↑(2分)
H2↑(2分)
Na+和H+(1分)
(3)NaCl+NH3+CO2+H2O NaHCO3+NH4Cl(2分) NH3(1分) NH3极易溶于NaCl溶液,而CO2在NaCl溶液中溶解度很小(2分)
NaHCO3+NH4Cl(2分) NH3(1分) NH3极易溶于NaCl溶液,而CO2在NaCl溶液中溶解度很小(2分)
(4)由于熔点MgO>MgCl2,电解MgO耗费电多,而电解MgCl2耗电较少(2分)
题目分析:
(1)蒸馏法、离子交换法、电渗析法(任选两个)
(2)2NaCl+2H2O电解2NaOH+H2↑+Cl2↑ 正 2H++2e- H2↑
H2↑
Na+和H+
(3)NaCl+NH3+CO2+H2O NaHCO3+NH4Cl NH3 NH3极易溶于NaCl溶液,而CO2在NaCl溶液中溶解度很小
NaHCO3+NH4Cl NH3 NH3极易溶于NaCl溶液,而CO2在NaCl溶液中溶解度很小
(4)由于熔点MgO>MgCl2,电解MgO耗费电多,而电解MgCl2耗电较少
