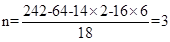问题
计算题
(6分)有一硝酸盐晶体,分子式为M(NO3)x·nH2O,经测定其摩尔质量为
242g / mol。取1.21 g此晶体溶于水,配制成100 mL溶液。将其置于电解池中用惰性材料为电极进行电解。经测定,当有0.01 mol电子通过电极时,溶液中全部金属离子即在阴极上析出,电极增重0.32 g。计算:(写出计算过程)
(1) 1.21 g此盐晶体的物质的量是多少?x值是多少?
(2) 求M的相对原子质量和n值。
答案
(1)0.005mol x=2 (2)M=64g/mol n=3
考查根据电解原理进行的有关计算。
(1) 该盐晶体的物质的量为=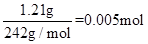
由 M-x e-=Mx+可知
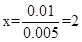
(2) 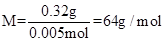
故原子量为64,即Cu。
则