(12分)
碳、硫的含量影响钢铁性能,碳、硫含量的一种测定方法是将钢样中碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下x克钢样中碳、硫转化为CO2、SO2。
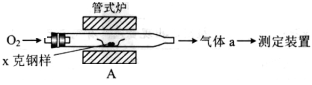
①气体a的成分是____________________。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5 O2高温1____+3_____。
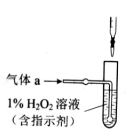
(2)将气体a通入测硫酸装置中(如右图),采用滴定法测定硫的含量。
①H2O2氧化SO2的化学方程式:_________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mLNaOH溶液,若消耗1mLNaOH溶液相当于硫的质量为y克,则该钢样中硫的质量分数:_________________。
(3)将气体a通入测碳装置中(如下图),采用重量法测定碳的含量。
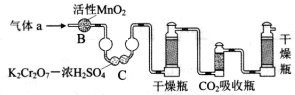
①气体a通过B和C的目的是_____________________。
②计算钢样中碳的质量分数,应测量的数据是__________________。
(1)①CO2、SO2、O2;②Fe3O4;SO2
(2)①H2O2+SO2=H2SO4;② zy/x
(3)①除去SO2对CO2测定的干扰
②吸收CO2气体前后吸收瓶的质量
题目分析:(1)①钢样中的碳、硫在装置A中被氧化为CO2、SO2,故a的成分为CO2、SO2以及未反应的O2;
②FeS中的,-2价的硫被氧化为SO2,+2价的Fe被氧化为+3价的铁,结合所给化学计量数,可知产物应为Fe3O4和SO2,故方程式为3FeS+5O2=Fe3O4+3SO2。
(2)①H2O2具有氧化性,可氧化SO2使S的化合价升高为+6价,在溶液中反应产物应为硫酸,故反应方程式为:H2O2+SO2=H2SO4;②1mL NaOH相当于yg S,故z mL NaOH相当于 zy g S,则该样品中硫的质量分数为zy/x 。
(3)①测定碳的含量需将气体a中的SO2除去,故装置B和C的作用是除去SO2;②计算碳的质量分数须利用CO2的质量进行分析,故需测量CO2吸收瓶在吸收CO2气体前后的质量。
