(15分)资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学通过如下实验探究反应原理并验证产物。
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
(1)该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[xMg(OH)2•yMgCO3]
(2)为了确定产物成份(包括产生的气体、白色不溶物及溶液中溶质),进行以下定性实验。请填写表中空白:
| 实验序号 | 实 验 | 实验现象 | 结 论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 安静燃烧,火焰呈淡蓝色 | 气体成分为 ① |
| 实验Ⅲ | 将实验I中的白色不溶物滤出、洗涤,取少量加入足量 ② | ③ | 白色不溶物中含有MgCO3 |
| 实验Ⅳ | 取实验Ⅲ中的滤液,向其中加入适 量 ④ 稀溶液 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO32-离子 |
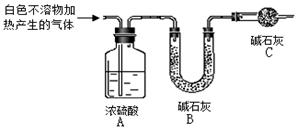
称取干燥、纯净的白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
①装置C的作用是 ;
②白色不溶物的化学式为 。
(4)根据以上(2)及(3)的定性定量实验,写出镁与饱和碳酸氢钠溶液反应的化学方程式
__________________________________________________________________________。
(1)猜测1: Mg(OH)2(2分)
(2)①氢气(或H2)(1分)
②稀盐酸(合理均可)(2分)
③产生气泡,沉淀全部溶解 (2分)
④CaCl2或BaCl2(2分)
(3)①防止空气中的水蒸气和CO2进入装置B中,影响实验结果(2分)
②Mg(OH)2•2MgCO3 或 Mg3(OH)2(CO3)2 (2分)
(4)3Mg+4NaHCO3+2H2O= Mg(OH)2• 2MgCO3↓+2Na2CO3+3H2↑(2分)
题目分析:⑴根据猜测2、3的内容可确定猜测1为“白色不溶物可能为Mg(OH)2”;
⑵实验Ⅱ:根据气体的火焰呈淡蓝色,可确定气体的成分为氢气;
实验Ⅲ:结合Mg(OH)2、MgCO3的性质,可用稀盐酸等与其反应,若产生气泡,且沉淀全部溶解,说明白色不溶物中含有MgCO3;
实验Ⅳ:要证明溶液中存在CO32-离子,可向实验Ⅲ的滤液中加入CaCl2或BaCl2,观察是否产生白色沉淀来证明;
⑶①装置末端用碱石灰吸收空气中水蒸气和CO2,防止其进入装置B中,影响实验结果;
②根据xMg(OH)2•yMgCO3的灼烧反应:xMg(OH)2•yMgCO3 (x+y)MgO+xH2O+yCO2
(x+y)MgO+xH2O+yCO2
有n(H2O)=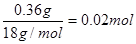 ;n(CO2)=
;n(CO2)=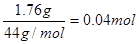 ,则x:y=1:2,即得白色不溶物的化学式为Mg(OH)2•2MgCO3或Mg3(OH)2(CO3)2。
,则x:y=1:2,即得白色不溶物的化学式为Mg(OH)2•2MgCO3或Mg3(OH)2(CO3)2。
⑷综上可得该反应的反应物有Mg、NaHCO3,生成物有Mg(OH)2• 2MgCO3、Na2CO3、H2,最后根据观察法将其配平。
