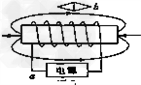
某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
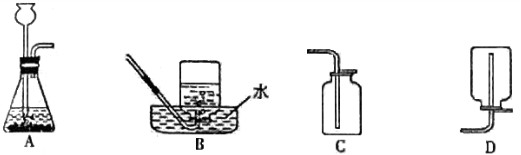
⑴上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳的化学方程式 ; 。
⑵请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.Cu和Cu2O均为不溶于水的红色固体;Ⅱ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含有Cu;假设二:红色固体只含Cu2O;
假设三: (请补充完成假设三)。
②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 成立 |
| b.取少量红色固体加入到足量硫酸溶液中 | 假设二和假设三均成立 |
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后, (填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m  (选填>、<或=),则假设二成立;若m
(选填>、<或=),则假设二成立;若m  (选填>、<或=),则假设三成立。
(选填>、<或=),则假设三成立。
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论。
⑴Zn+H2SO4=ZnSO4+H2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑
⑵①红色固体含有Cu和Cu2O两种物质; ②一;溶液由无色变为蓝色 ③过滤;=;>
题目分析:(1)实验室常用锌粒与稀硫酸反应制取氢气,同时还生成硫酸锌,故反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑;实验室常用石灰石或大理石与稀盐酸反应制取二氧化碳,同时还生成氯化钙和水,故反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑。
(2)①根据题意,氢气还原氧化铜有可能生成铜或氧化亚铜,故可猜想反应后的生成物为:铜、或氧化亚铜、或铜与氧化亚铜的混合物。
②由于铜属于H后金属,故稀硫酸不能与铜发生反应;而根据资料可知,氧化亚铜能与稀硫酸反应生成铜、硫酸铜和水;因此,当取少量红色固体加入到足量硫酸溶液中,a若无现象时,说明固体中只含有铜;而b若溶液变成蓝色时,则说明红色固体中含有氧化亚铜,即假设二和假设三均成立。
③根据题意,要从溶液中得到不溶于液体的剩余的红色固体,需先进行过滤,然后再洗涤、干燥。
若假设二成立,则红色固体中只含Cu2O,那么Wg红色固体(Cu2O)都能与足量稀硫酸反应,据此,根据Cu2O的质量Wg,可计算出剩余固体(Cu)m的质量。
解,假设Wg红色固体全部是Cu2O,反应后生成铜的质量为m,则
Cu2O+H2SO4=Cu+CuSO4+H2O
144 64
W m
144:64=W:m
解得,m=
即当m= 时,假设二成立。
时,假设二成立。
若m> 时,则说明红色固体中原本就含有铜,所以假设三成立。
时,则说明红色固体中原本就含有铜,所以假设三成立。
点评:对于验证型实验探究,要熟记物质的性质或变化规律,根据给出的实验设计方案,进行实验、分析和探究,并通过观察、记录和分析的实验现象,来验证该物质的性质或变化规律等。