某中学化学实验室有如图所示的实验装置,用于制取氧气、二氧化碳等多种气体.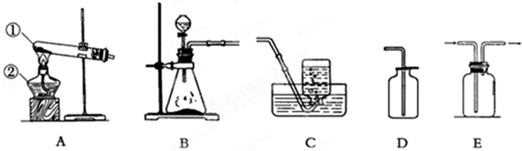
(1)请写出有标号仪器的名称:① ②
(2)若制取的一种气体是 ,应选用的收集装置是 (填序号,下同),应选用的发生装置是 ,反应的化学方程式是 ;检验所制取的气体的方法是: ;
(3)在常温下,用亚硫酸钠固体和稀硫酸制取二氧化硫气体,应选用的发生装置是: ;由于二氧化硫是易溶于水、密度比空气大的有毒气体,所以应用 装置进行收集,以便将尾气吸收处理,避免造成
(4)该中学化学课外兴趣小组同学利用发生装置B进行“石块中是否含有碳酸钙”的探究活动.在活动中小明发现,相邻小组气体产生的速率比自己小组的快.小明将这一情况报告老师,老师鼓励他们对此问题共同探究.
【提出问题】影响二氧化碳气体产生速率的因素是什么?
【作出猜想】①不同地点石块中碳酸钙含量不同;
②所用的盐酸不同;
③还可能是 .
【设计实验】(1)验证猜想①是否成立,要设计的实验:分别取大小相同、质量相同、 的石块,加入相同的稀盐酸进行实验.
【交流讨论】实验中可以通过观察 ,粗略地比较反应速率.
【拓展延伸】上述实验中,小明采用了控制单一变量的研究方法.用此方法探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有 等(答出一点即可).
(1)试管;酒精灯;
(2)氧气;C或D;A;2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)B;E;大气污染;
(4)石块大小不同(或石块质量不同、盐酸质量不同);
不同地点;
放出气泡的剧烈程度不同;过氧化氢溶液的浓度、温度(合理均可).
题目分析:(1)依据常用仪器回答;
(2)若制取的是氧气,据氧气的密度和溶解性确定收集装置,并据制取氧气的方法书写方程式,选择发生装置;检验氧气用带火星的木条伸入瓶内,若木条复燃则是氧气;
(3)根据反应物状态和反应条件选择发生装置;并据二氧化硫的性质选择收集装置;
(4)【作出猜想】③从药品的表面积和酸的质量分数考虑;
【设计实验】(1)控制不同地点是石块这一个变量;
【交流讨论】实验中可以通过观察放出气泡的剧烈程度不同,粗略地比较反应速率;
【拓展延伸】从实验所需要的条件的考虑.
解:(1)标号仪器分别是试管和酒精灯;
(2)根据题意,这些装置可用于制取氧气和二氧化碳,若制取的是氧气,氧气的密度比空气大且不易溶于水,则可用向上排空气法或排水法收集;制取氧气可用加热高锰酸钾或氯酸钾的方法,分解过氧化氢溶液的方法,若用加热高锰酸钾的方法,属于固体加热型,则选A发生装置;反应方程式是2KMnO4 K2MnO4+MnO2+O2↑;检验氧气用带火星的木条伸入瓶内,若木条复燃则是氧气;
K2MnO4+MnO2+O2↑;检验氧气用带火星的木条伸入瓶内,若木条复燃则是氧气;
(3)常温下,用亚硫酸钠固体和稀硫酸制取二氧化硫气体,不需加热,属于固液常温型,故选发生装置B;由于二氧化硫是易溶于水、密度比空气大的有毒气体,所以应用E收集,可将尾气用水吸收,防止污染大气;
(4)【作出猜想】③影响二氧化碳产生速率的因素还可能是:石块大小不同(或石块质量不同、盐酸质量不同);
【设计实验】(1)验证猜想①是否成立,要设计的实验:其他量都要相同,但要取不同地点的石块,进行实验;
【交流讨论】实验中可以通过观察气泡产生的剧烈程度,粗略地比较反应速率;
【拓展延伸】探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有 温度、溶液的溶质质量分数、溶液质量、压强等;
故答案为:(1)试管;酒精灯;
(2)氧气;C或D;A;2KMnO4 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)B;E;大气污染;
(4)石块大小不同(或石块质量不同、盐酸质量不同);
不同地点;
放出气泡的剧烈程度不同;过氧化氢溶液的浓度、温度(合理均可).
点评:掌握装置选取方法,反应原理,并能灵活应用解答问题,通过控制变量的方法研究化学问题是一种常用的方法,同学们要学会如何控制一个反应的变量,明确哪些变量可以控制等.
