某学习小组围绕“实验室制取气体”进行研讨。请你参与完成下面的问题。
(1)原理分析:实验室制取CO2的化学方程式为 。
不用碳酸钠与盐酸反应制取CO2的原因是 。
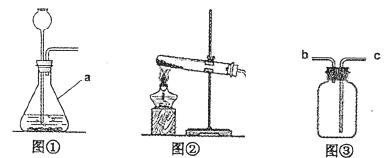
(2)发生装置:图①装置中仪器a的名称是 。实验室常用无水醋酸钠固体与碱石灰在加热的情况下制甲烷,其发生装置应选图 (填序号)。
(3)收集装置:实验室收集氨气应采用的方法是 。收集有毒气体二氧化硫时,常采用图③收集装置,气体应从 (填字母)端通入。
(4)实验操作:通常实验室制取氢气选择的发生装置是 (填序号),检查该装置气密性的操作是 。若利用图③用排水法收集氢气,则水从 (填字母)端排出。
(5)实验反思:在加热氯酸钾制O2的过程中,发现产生O2的速率很慢,经检查不是氯酸钾变质,也不是装置气密性不好,你认为最可能的原因是 。
(1)CaCO3+2HCl=CaCl2+H2O+CO2↑ 反应快,不易控制
(2)锥形瓶 ②
(3)向下排空气法 c
(4)① 先将长颈漏斗进行液封,然后将导管的一端放入水中,双手紧握仪器外壁,若导管口有气泡冒出即气密性良好。(或先用止水夹夹住橡皮管,然后往长颈漏斗中加入水至形成一段高于试管内液面的水柱,静置水柱高度不变,则装置气密性好。) c
(5)未加MnO2(或未加催化剂)
题目分析:(1)实验室常用大理石和稀盐酸反应制取二氧化碳,同时还生成氯化钙和水,故反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;由于碳酸钠与盐酸反应的速度过快,故不易控制。
(2)根据实验室常用仪器回答,图①装置中仪器a的名称是锥形瓶;根据题意,实验室常用无水醋酸钠固体与碱石灰在加热的情况下制甲烷,故属于“固体加热型”,其发生装置应选图②。
(3)由于氨气的相对分子质量小于空气的平均分子质量,故可知其密度小于空气,又因为氨气极易溶于水,故只能用向下排空气法收集;由于二氧化硫的密度大于空气,故若用图③收集装置收集时,气体应从长管c进入,从下向上排空气。
(4)实验室常用固体锌粒和稀硫酸在常温下反应,制取氢气,故属于“固液体不加热型”,其发生装置应选图①。根据气密性检查的原理分析,装置的气密性检查,是利用给装置受热,使其内部气压增大而实现的,而由于该装置有两个出口,故检查气密性时,应先堵住一个出口;如先将长颈漏斗进行液封,然后将导管的一端放入水中,双手紧握仪器外壁,若导管口有气泡冒出即气密性良好。(或先用止水夹夹住橡皮管,然后往长颈漏斗中加入水至形成一段高于试管内液面的水柱,静置水柱高度不变,则装置气密性好。)由于氢气的密度小于水,故若利用图③用排水法收集氢气,氢气应从短管b进入,从上往下排水,则水会从长管c排出。
(5)由于氯酸钾要在二氧化锰作催化剂和加热的条件下,分解生成氯化钾和氧气,结合题意可知,产生O2的速率很慢的原因应是未加催化剂。
点评:熟记氧气和二氧化碳的实验室制法、原理和操作注意事项,是解题的关键;此外,本题的重点是常用气体的发生装置和收集装置的选取方法,要学会根据反应物的状态和反应的条件选择发生装置,根据制取气体的溶解性和密度的大小选择收集气体的方法。
