高锰酸钾是一种重要的化学试剂,其溶液不很稳定,在酸性条件下会分解生成二氧化锰和氧气,在中性或弱碱性溶液中分解速度很慢,见光分解速度加快。
(1)高锰酸钾溶液应________________(填保存的注意事项);酸性条件下高锰酸钾溶液分解的离子方程式______________。
(2)请配平高锰酸钾溶液与草酸钠Na2C2O4溶液在酸性条件下反应的离子方程式:____MnO4- + ____C2O42-+ ____ H+ —— ____Mn2+ + ______CO2↑+ _______
(3)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴地滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡时),记录的现象如下表:
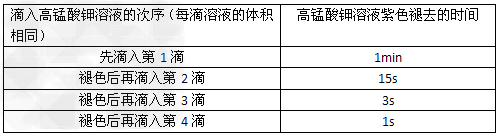
请分析高锰酸钾溶液褪色时间变化的原因________________。
(4)该学习小组在获取了上述经验和结论以后,用稳定的物质草酸钠Na2C2O4(相对分子质量134.0)来标定高锰酸钾溶液的浓度。他们准确称取1.340g纯净的草酸钠配成250mL溶液,每次准确量取25.00mL溶液酸化后用KMnO4溶液滴定。
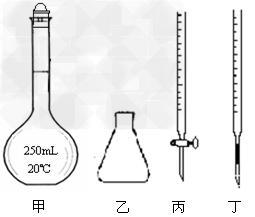
①高锰酸钾溶液应装在________(填下图中的仪器编号)。
②为了防止高锰酸钾在酸性条件下分解而造成误差,滴定开始时,操作上必须是______________。
③当溶液呈微红色且半分钟内不褪色,消耗KMnO4溶液20.00mL(多次测定的平均值),则KMnO4溶液的浓度为________________。(附原子相对质量K=39Mn=55O=16 Na=23C=12)
(1)配成中性溶液并保存在棕色试剂瓶中 ;4MnO4-+4H+ === 4MnO2↓+3O2↑+2H2O
(2)2 ; 5 ;16 ==== 2 ;10 ; 8H2O
(3)反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好
(4)①丙
②逐滴滴入高锰酸钾溶液,待前一滴高锰酸钾溶液颜色褪去后再滴加 (说明:当溶液中生成的Mn2+较多时,反应速率加快后再增大滴加速度)
③0.0200mol/L
