(15分)(1)3.01×1022个OH¯的物质的量为 ;这些OH¯与 molNH3的质量相等,与 g Na+含有的离子数相同。
(2)在标准状况下,2.24LNOx气体的质量为4.6g,则x的值为 。
(3)有四种正盐的混合溶液,含有0.2 mol·L-1 Na+、0.25 mol·L-1 Mg2+、0.4mol·L-1
Cl-,则SO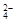 的浓度为
的浓度为
(4)、用14.2g硫酸钠配制成500mL溶液,其物质的量浓度为 mol/L。若从中取出50mL,其物质的量浓度为 mol/L,溶液中含Na+的个数为
若将这50mL溶液用水稀释到100mL, SO42-的物质的量浓度为 mol/L。
(1)0.05, 0.05,1.15 (每空1分)
(2)2 (2分) (3)0.15mol/L (2分)
(4) 0.2 mol/L、 0.02NA、0.2mol/L、0.1 mol/L。(每空2分)
(1)3.01×1022个OH¯分子的物质的量是3.01×1022÷6.02×1023/mol=0.05mol,氨气的摩尔质量与OH¯的摩尔质量相同,所以氨气的物质的量是0.05mol。钠离子的物质的量是0.05mol,质量是0.05mol×23g/mol=1.15g。
(2)标准状况下,2.24LNOx气体的物质的量是0.1mol,则该气体的相对分子质量是46,所以x=2。
(3)溶液是电中性的,所以SO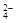 的浓度为(0.2 mol·L-1+2×0.25 mol·L-1 -0.4mol·L-1)÷2=0.15mol/L。
的浓度为(0.2 mol·L-1+2×0.25 mol·L-1 -0.4mol·L-1)÷2=0.15mol/L。
(4)14.2g硫酸钠的物质的量是14.2g÷142g/mol=0.1mol,则根据c=n/V可知,浓度是0.1mol÷0.5L=0.2 mol/L;溶液是均一的,因此浓度不变;溶液中含Na+的个数为0.05L×0.4mol/L×NA=0.02NA;在稀释过程中,溶质是不变的,所以稀释后的浓度是0.2mol/L÷2=0.1 mol/L。
