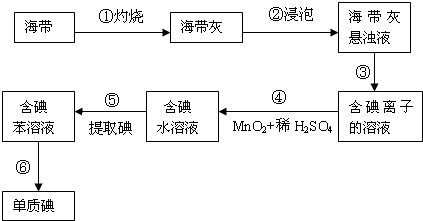
海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
(1)步骤④中需用到1mol/L的稀硫酸100mL,若用98%,密度为1.84g/cm3的浓硫酸来配制,则应用量筒量取浓硫酸的体积是______.
(2)步骤③的实验操作名称是______;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是______.
(3)步骤⑤中选择用苯而不用酒精来提取碘的理由是______.
(4)查阅资料:该小组同学知道海带中的碘元素主要以有机碘化物的形式存在,若该小组实验时称得海带的质量为ag,提取碘的过程中碘损失了m%,最后得到单质碘的质量为bg,该小组同学测得的海带中碘的含量为(用含a、b、m的式子表示)______.
(1)浓硫酸的物质的量浓度为
=103ρw M
mol/L=18.4mol/L;设需要浓氢氧化钠溶液的体积为V,0.2mol/L×0.5L=18.4mol/L×V,V=0.0054L=5.4mL,103×1.84×98% 98
故答案为:5.4mL;
(2)步骤③是分离固体和液体,则实验操作为过滤,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,是利用互溶的两种液体的沸点不同来分离,则实验操作为蒸馏,
故答案为:过滤;蒸馏;
(3)酒精与水互溶而苯不溶于水,故答案为:酒精溶于水而苯不溶于水;
(4)总的碘单质的质量为
,则海带中碘的质量分数为b (1-m%)
%,故答案为:100b a(1-m%)
%或b a(1-m)
%.100b a(1-m%)
