Discover
Newsmagazine of science, devot ed to the wonders and stories of modern science, is written for the educated general reader. Published(出版) by Disney Magazine Publishing Co., Discover tells many of the same stories professionals(专业人员) read in Scientific American. A truly delightful family science magazine, each issue(每期) brings to light new and newsworthy topics to make dinnertime and water-cooler conversations interesting.
ed to the wonders and stories of modern science, is written for the educated general reader. Published(出版) by Disney Magazine Publishing Co., Discover tells many of the same stories professionals(专业人员) read in Scientific American. A truly delightful family science magazine, each issue(每期) brings to light new and newsworthy topics to make dinnertime and water-cooler conversations interesting.
Cover Price: $59.88
Price: $19.95($1.66/issue)
You Save: $39.93(67%)
Issues: 12 issues/12 months
Self
Published by Conde Nast Publications Inc., Self is a handbook devoted to women’s overall physical and mental health. Every issue contains usable articles such as “Style Lab”, in which wearable clothes are mixed and matched on non-models and the “Eat-right Road Map”, with tips on how to eat properly.
Cover Price: $35.86
Price: $15.00($2.5/issue)
You Save: $20.86(58%)
Issues: 10 issues/12 months
Instyle
Instyle is a guide to the lives and lifestyles of the world’s famous people. The magazine covers the choices people make about their homes, their clothes and their free time activities. With photos and articles, it opens the door to these people’s homes, families, parties and weddings, offering ideas about beauty, fitness and in general, lifestyles. Publisher: The Time Inc.Magazine Company.
Cover Price: $47.88
Price: $23.88($2.38/issue)
You Save: $24.00(50%)
Issues: 10 issues/12 months
Wired
This magazine is designed for leaders in the field of information engineering, including top managers and professionals in the computer, business, design and education industries. Published by Conde Nast Publications Inc., Wired often carries articles on how technology changes people’s lives.
Cover Price: $59.40
Price: $10.00($1.00/issue)
You save: $49.40(83%)
Issues: 10 issues/12months
小题1:Which of the following magazines is published monthly?
A.Discover
B.Self
C.Instyle
D.Wired小题2:Which two magazines are published by the same publisher?
A.Wired and Instyle
B.Discover and Instyle
C.Self and Discove
D.Self and Wired小题3:Which magazine offers the biggest price cut?
A.Instyle
B.Wired
C.Discover
D.Self小题4:Those who are interested in management and the use of high technology would probably choose _____.
A.Instyle
B.Self
C.Wired
D.Discover
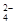 的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO
的物质的量浓度是多少?H+的物质的量浓度是多少?溶质的质量是多少?此溶液中含 H+的物质的量是少?其中含有多少个 SO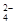 ?
?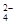 )= c(H2SO4)=" 2" mol/L;
)= c(H2SO4)=" 2" mol/L;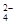 )=" 0.6" mol,
)=" 0.6" mol,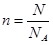 可知
可知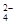 )=" 0.6" mol×6.02×1023 mol-1 = 3.612×1023。
)=" 0.6" mol×6.02×1023 mol-1 = 3.612×1023。
 ed to the wonders and stories of modern science, is written for the educated general reader. Published(出版) by Disney Magazine Publishing Co., Discover tells many of the same stories professionals(专业人员) read in Scientific American. A truly delightful family science magazine, each issue(每期) brings to light new and newsworthy topics to make dinnertime and water-cooler conversations interesting.
ed to the wonders and stories of modern science, is written for the educated general reader. Published(出版) by Disney Magazine Publishing Co., Discover tells many of the same stories professionals(专业人员) read in Scientific American. A truly delightful family science magazine, each issue(每期) brings to light new and newsworthy topics to make dinnertime and water-cooler conversations interesting.