问题
实验题
某同学利用如图所示装置来制取Fe(OH)3胶体。
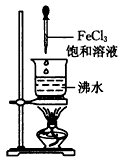
[原理分析]实验室制备胶体一般是利用盐类的水解或酸、碱、盐之间的复分解反应。Fe(OH)3胶体就是采用三价铁盐水解的方法来制备的。
[实验设计]在小烧杯中加入25 mL蒸馏水,加热至沸腾,慢慢滴入1~2 mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热,即可得Fe(OH)3胶体。实现现象:烧杯中液体呈红褐色。化学方程式:
FeCl3+3H2OFe(OH)3(胶体)+3HCl
(1)实验中必须要用蒸馏水,而不能用自来水。原因是_________________。
(2)实验操作中,必须选用饱和氯化铁溶液而不能用稀氯化铁溶液。原因是______________________。
(3)往沸水中滴加饱和氯化铁溶液后,可稍微加热煮沸,但不宜 长时间加热。这样操作的原因是______________________。
答案
(1)自来水中含电解质、杂质较多,易使制备的胶体马上发生聚沉,导致实验失败
(2)氯化铁溶液浓度过稀不利于氢氧化铁胶体的形成
(3)长时间加热会导致氢氧化铁胶体聚沉
