结合如图所示的实验装置,回答有关问题:
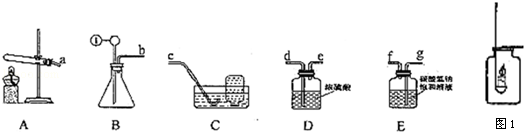
(1)写出标号①的仪器名称 ;
(2)若用A装置来制备O2,有关反应可用化学方程式表示为 ;
(3)如图1所示,蜡烛在氧气中燃烧,然后加入澄清石灰水,即可验证蜡烛中含有碳、氢元素。若使用C装置收集氧气,就不能得出正确结论,原因是 ;
(4)用大理石和盐酸反应,选用图中适当的装置加以组合,制出纯净、干燥的CO2,则所选装置各接口的连接顺序为 ,反应原理的化学方程式为 。
(1)长颈漏斗;(2)2KClO3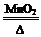 2KCl+3O2↑;
2KCl+3O2↑;
(3)排水法收集的氧气中混有水蒸气,无法判断燃烧是否生成水,也就无法验证蜡烛中是否含有氢元素;(4)b→g→f→d→e;CaCO3+2HCl=CaCl2+CO2↑+H2O
题目分析:(1)据常用仪器回答;标号①是添加液体的长颈漏斗;
(2)用A装置来制备O2,属于加热固体型,试管口无棉花,说明是用加热氯酸钾的方法制取氧气,方程式是:2KClO3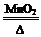 2KCl+3O2↑;
2KCl+3O2↑;
(3)化学反应前后元素的种类不变,据生成物的元素组成推测反应物的组成是解答的思路,同时要注意排除干扰因素,然后结合题意分析判断;蜡烛在氧气中燃烧,集气瓶壁上会有水雾生成,然后加入澄清石灰水,石灰水变浑浊,说明蜡烛燃烧生成二氧化碳和水,据反应前后元素种类不变,即可验证蜡烛中含有碳、氢元素,若使用C装置收集氧气,排水法收集的氧气中会混有水蒸气,无法判断燃烧是否生成水,也就无法验证蜡烛中是否含有氢元素;
(4)要制取干燥、纯净的二氧化碳,可用饱和的碳酸氢钠溶液除去气体中混有的氯化氢气体,浓硫酸进行干燥,由于气体从溶液中出来会带来水蒸气,所以要除杂质气体再干燥收集,同时注意洗气装置中导管要长进短出,并据大理石和稀盐酸反应原理书写方程式。由于盐酸具有挥发性,使制得的CO2中混有一些氯化氢气体.所以此题的关键是除掉CO2气体中混有的HCl气体,并进行干燥;选用碳酸氢钠溶液可除掉混有的HCl气体,且生成的CO2气体没影响.二氧化碳的干燥选择浓硫酸即可。而端口的连接应从长导管进入,这样才能起到净化和干燥的目的,干燥完毕可用向上排空气法收集,因为二氧化碳的密度比空气大,故连接顺序为b→g→f→d→e;大理石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+CO2↑+H2O。
