(15分)某研究小组用黄铜矿(主要成分是CuFeS2,其中S为-2价)为主要原料炼铜,其总反应为:2CuFeS2+2SiO2+5O2=2Cu+2FeSiO3+4SO2。事实上该反应是按如下流程分步进行的:


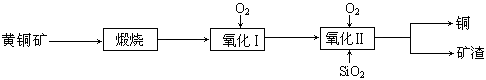
(1)氧化Ⅰ的反应主要是煅烧生成的硫化亚铁被进一步氧化为氧化亚铁,并与二氧化硅反应生成矿渣。矿渣的主要成分是 (填化学式)。
(2)据报道,有一种细菌在氧气存在下可以将黄铜矿氧化成硫酸盐,反应是在酸性溶液中发生的。该反应的化学方程式为 。
(3)我国学者研究发现,以精CuFeS2矿为原料在沸腾炉中与O2(空气)反应,生成物冷却后经溶解、除铁、结晶,得到CuSO4·5H2O,生产成本能够降低许多。有关实验结果如下表:
| 沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 |
| 水溶性Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 |
②实际生产过程中沸腾炉温度为600~620 ℃。则控制温度的方法是 。
③当温度高于600~620 ℃时,生成物中水溶性铜下降的原因是 。
④生成物冷却后的除铁的实验操作方法主要是 。已知在溶液中,Cu2+开始沉淀和沉淀完全的pH分别为4.7、6.7,Fe3+开始沉淀和沉淀完全的pH分别为1.1、3.2;如果制得的硫酸铜溶液中含有少量的Fe3+,请写出除去溶液中Fe3+的实验操作步骤: 。
共15分
(1)FeSiO3(2分)
(2)4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O(2分)
4CuSO4+2Fe2(SO4)3+2H2O(2分)
(3)①4CuFeS2+15O2=4CuSO4+2Fe2O3+4SO2(2分)
②控制加入CuFeS2的速度(因CuFeS2与O2反应放热)(2分)
③CuSO4受热分解(2分)
④过滤(2分) 加入CuO[或Cu(OH)2或CuCO3]粉末,充分搅拌,调节溶液的pH约为3.2,加热煮沸,过滤,用(适量)稀硫酸酸化(3分)
题目分析:(1)根据2CuFeS2+2SiO2+5O2=2Cu+2FeSiO3+4SO2,可得矿渣为FeSiO3;
(2)由题意可知,CuFeS2在酸性溶液中与氧气在一种细菌的作用下生成的硫酸盐是硫酸铜和硫酸铁,化学方程式为4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O;
4CuSO4+2Fe2(SO4)3+2H2O;
(3)①精CuFeS2矿为原料在沸腾炉中与O2(空气)反应,最终得CuSO4·5H2O,说明铁元素的存在形式是氧化铁,加水溶解可过滤除去,所以CuFeS2与O2反应的化学方程式为4CuFeS2+15O2=4CuSO4+2Fe2O3+4SO2
②因为CuFeS2与O2反应放热,所以在生产过程中控制加入CuFeS2的速度,控制温度;
③水溶性铜化合物为CuSO4•5H2O,酸溶性铜化合物为CuO,温度较高时,CuSO4•5H2O可分解生成CuO,则在600℃以上时水溶性铜化合物含量减少;
④生成物中除硫酸铜外还有氧化铁,氧化铁不溶于水,所以冷却后的除铁的实验操作方法主要是过滤;除去铁离子而不除去铜离子,调节溶液的pH值在3.2到4.7之间,使铁离子完全沉淀,而铜离子不沉淀,所以具体操作是加入CuO[或Cu(OH)2或CuCO3]粉末,充分搅拌,调节溶液的pH约为3.2,加热煮沸,过滤,用(适量)稀硫酸酸化。


