(1)在标准状况下,气体A的密度为1.25g/L,气体B相对于氢气的密度为21, 若8.96LA和B的混合气体的质量为13.44g,则混合物中A与B的体积比为 。
(2)同温同压下的SO2与氦气,若质量相同,两种气体的体积比为 ;若体积相同时,两种气体的质量比为 。
(3)将炭粉与wg氧气置于密闭容器中,经高温充分反应后,恢复到初始温度,测得反应前后压强分别为Po、P.已知:P=nPo,加入炭粉质量xg与n的变化关系如图。
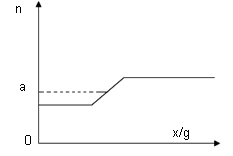
①n的最小值为 ,此时x的取值范围为 g。②n的最大值为 ,此时x的取值范围为 g。③若实验测得n值为a,则容器内CO2和CO的体积比为 。
(8分)(1)3:2 (2) 1:16 16:1
(3)①1 0<x≤3w/8 ②2 x≥3w/4 ③(2-a)/2(a-1)
(1)设混合物中A与B的物质的量分别是x和y,则x+y=8.96L÷22.4L/mol=0.4mol。在标准状况下,气体A的密度为1.25g/L,则A的相对分子质量是1.25×22.4=28;气体B相对于氢气的密度为21, 则B的相对分子质量是42,所以28x+42y=13.44g,解得x=0.24mol,y=0.16mol,则混合物中A与B的体积比为3:2。
(2)在质量相等的条件下,SO2和氦气的物质的量之比是4︰64=1︰16。根据阿伏加德罗定律可知,二者的体积之比是1︰16。在体积相等的条件下,二者的物质的量之比是1︰1,因此二者的质量之比是16︰1。
(3)①Wg氧气的物质的量是W/32mol。反应中可能发生的反应有C+O2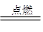 CO2、2C+O2
CO2、2C+O2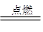 2CO。所以n的最小值是1,此时碳的物质的量小于或等于W/32mol,因此X的取值范围是0<x≤3w/8。
2CO。所以n的最小值是1,此时碳的物质的量小于或等于W/32mol,因此X的取值范围是0<x≤3w/8。
②根据反应的方程式可知,n的最大值是2,此时碳的物质的量大于或等于W/32mol,因此X的取值范围是x≥3w/4。
③反应V = a时容器里有CO和CO2两种气体,设它们的体积分别是V1,V2
则0.5V1+V2 = V(O2)
V1+V2 = aV(O2)
所以a(0.5V1+V2) = V1+V2
V1 : V2 = (1-a) : (0.5a-1)。