问题
计算题
(8分)32g铜与150mL一定浓度的硝酸恰好完全反应,产生的NO2和NO混合气体在标准状况下的体积为11.2L.请回答:(不要求写计算过程)
(1)写出铜与稀硝酸反应的化学方程式
(2)NO为 mol.标准状况V(NO):V(NO2)=
(3)原硝酸溶液的浓度为 mol•L-1
(4)试描述实验过程中试管内产生气体现象
答案
(1)3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)0.25,1:1; (3)10; (4)气体颜色逐渐变浅.
题目分析:(1)写出铜与稀硝酸反应的化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)设NO2的物质的量为x,NO的物质的量为y,则有
x+y=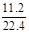
x+3y=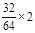
解得:x=0.25mol y=0.25mol
则V(NO):V(NO2)=1:1
(3)铜与硝酸恰好反应,根据N原子守恒,n(HNO3)=n(NO3-)+n(气体),又知n(Cu2+)=0.5mol,所以n(NO3-)=1mol,则n(HNO3)=1.5mol,c(HNO3)=" 10" mol•L-1。
(4)随着硝酸变稀,产生的NO2变少,NO变多,所以实验过程中试管内产生气体的现象是气体颜色逐渐变浅。
点评:原子守恒解本题比较简单。
