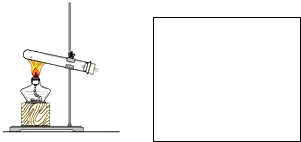
Ⅰ.写出实验室制氨气的化学方程式:______.
在如图所示的方框内画出氨气的收集装置(夹持装置可略去)
Ⅱ.
(1)浓硫酸与木炭粉在加热条件下反应.已知酸性KMnO4溶液可以吸收SO2,试用如表所示的各装置设计一个实验,验证上述反应所产生的各种产物.
| 编号 | ① | ② | ③ | ④ |
| 装置 | 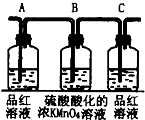 | 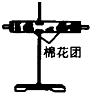 | 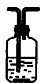 | 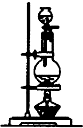 |
______→______→______→______.
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是______,B瓶溶液的作用是______,C瓶溶液的作用是______.
(3)装置②中所加的固体药品是______,可确证的产物是______,确定装置②在整套装置中位置的理由是______.
Ⅰ.实验室用氯化铵和氢氧化钙在加热条件下制取氨气,反应方程式为:2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑,氨气和极易溶于水,所以不能用排水法收集,常温下,氨气和氧气不反应,且氨气密度小于空气,所以可以采用向下排空气法收集,其收集装置图为:△ . 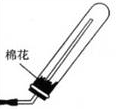 ,
,
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑,△ .  ;
;
Ⅱ(1)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,则其连接顺序是:④→②→①→③
,故答案为:④→②→①→③;
(2)A为检验二氧化硫装置,B、C为除去二氧化硫并检验是否除尽二氧化硫的装置,
故答案为:检验SO2气体,吸收SO2气体,检验SO2气体是否除净;
(3)无水硫酸铜为白色固体,遇水可变为五水硫酸铜(CuSO4•5H2O)为蓝色固体,用于检验水的存在,由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前,
故答案为:无水CuSO4,水蒸气,由于产物气流通过①、③时会带出水蒸气,所以②必须在①、③之前.
