根据下图回答有关问题.
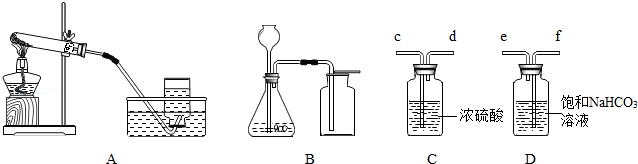
(1)实验室利用A装置制取氧气,当伸入集气瓶的导管口气泡 放出时,才可以收集氧气.用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是 .
(2)实验室利用B装置制取二氧化碳,该反应的化学方程式是 .制得的二氧化碳中含有 和氯化氢等杂质气体,可分别用C、D装置除去,则C、D的连接顺序是:混合气体→ (用接口字母表示).
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶,一段时间后,测得溶液的pH (填“>”、“<”或“=”)7,对该现象的合理解释是 (用化学方程式表示).
(1)连续、均匀; 吸收二氧化硫,防止污染空气;(2)CaCO3+2HCl=CaCl2+CO2↑+H2O; 水蒸气; fecd;(3)<;CO2+H2O=H2CO3.
题目分析:(1)实验室利用A装置制取氧气,当伸入集气瓶的导管口气泡连续、均匀冒出再开始收集,因为开始出来的气体是试管内的空气,立即收集会造成收集的氧气不纯;二氧化硫有毒,可与氢氧化钠溶液反应,所以集气瓶内放氢氧化钠溶液的目的是吸收二氧化硫,防止污染空气;(2)实验室用大理石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O;该反应生成水,且气体从溶液中出来会带来水蒸气,所以除杂质气体时先除氯化氢气体,再除水蒸气,且洗气装置长进短出;(3)二氧化碳可用水反应生成碳酸,使溶液显酸性,酸性溶液的pH值<7,反应方程式是:CO2+H2O=H2CO3;
