Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如下图所示的实验装置进行实验(夹持装置略去).圆底烧瓶A中的反应方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,请回答下列问题
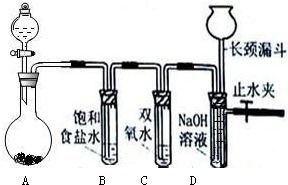
(1)试管B中饱和食盐水的作用______;
(2)试管C中加入5mL30%双氧水,发生反应的化学方程式______;
(3)试管D中充满10%NaOH溶液,NaOH溶液的作用是______;
(4)将浓盐酸注入圆底烧瓶A,当装置中的空气基本排尽后关闭止水夹,反应一段时间后试管D中的现象为______,试管D中的气体检验方法为______;
(5)有的同学对上述实验中试管D中气体来源产生质疑,你认为可能的来源有______(用化学方程式表示),对于质疑可以采用对比实验来解决.
(1)该实该验采用高锰酸钾固体和浓盐酸的方法制取氯气,产生的氯气中容易混有氯化氢气体,要除去氯化氢气体,所选的除杂试剂只能吸收氯化氢而不能吸收氯气,故可以使用饱和食盐水将其除去,
故答案为:除去Cl2中混有的HCl;
(2)Cl2氧化能力强于H2O2,试管C中氯气氧化过氧化氢生成氧气,自身被还原成氯化氢,反应为:Cl2+H2O2=2HCl+O2,
故答案为:Cl2+H2O2=2HCl+O2;
(3)氯气是一种有剧烈刺激性气味、有毒的气体,须进行尾气处理,试管D中充满10%NaOH溶液,氯气跟NaOH溶液反应Cl2+2NaOH=NaCl+NaClO+H2O,吸收多余的Cl2,
故答案为:吸收多余的Cl2;
(4)Cl2+H2O2=2HCl+O2,当关闭止水夹,反应一段时间后试管D中因氧气不断增多,气体压强增大,所以试管D中液面下降,长颈漏斗中液面上升,氧气使带火星的木条复燃,可用此法验证氧气,
故答案为:试管D中液面下降,长颈漏斗中液面上升;该气体能使带火星的木条复燃,证明是氧气;
(5)试管D中气体来源可能为过氧化氢的分解2H2O2=2H2O+O2↑,也可能为氯气氯气和水反应生成盐酸和次氯酸,次氯酸分Cl2+H2O=HCl+HClO;2HClO
2HCl+O2↑,光照 .
故答案为:2H2O2=2H2O+O2↑、Cl2+H2O=HCl+HClO、2HClO
2HCl+O2↑;光照 .
