某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液测定中和热.测定中和热的实验装置如图1所示.
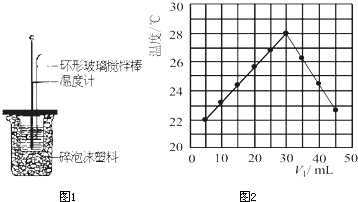
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):______.
(2)取50mLNaOH溶液和30mL硫酸溶液进行实验,数据如下表所示:
①请填写下表中的空白:
| 温度 | 起始温度t1/℃ | 终止温度 t1/℃ | 温度差 (t2-t1)t1/℃ | ||
| 实验次数 | H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验结果的数值与57.3kJ/mol有偏差,产生偏差的原因可能是______(填字母).
①室温低于10℃时进行实验,②在量取NaOH溶液的体积时仰视读数,③分多次把NaOH溶液倒入盛有硫酸的小烧杯中,④实验时用环形铜丝搅拌棒代替环形玻璃搅拌棒.
(3)将V1mL 0.4mol/LH2SO4溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图2所示(实验中始终保持V1+V2=50mL).下列叙述正确的是______
A做该实验时环境温度为22℃
B该实验表明化学能可转化为热能
CNaOH溶液的浓度约为1.2mol/L
D该实验表明有水生成的反应都是放热反应.
(1)已知稀强酸、稀强碱反应生成1mol液态水时放出57.3kJ的热量,稀硫酸和稀氢氧化钠溶液都是强酸和强碱的稀溶液,则反应的热化学方程式为:NaOH(aq)+HCl (aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol,
故答案为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)①第2组数据明显有误,所以删掉,三次温度差平均值=
=4.0C,故答案为:4.0;(30.1-26.1)+(29.8-25.9)+(30.4-26.3) 3
②50mL0.50mol/L氢氧化钠与30mL0.50mol/L硫酸溶液进行中和反应生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为:80ml×1g/ml=80g,温度变化的值为△T=4℃,则生成0.025mol水放出的热量为Q=m•c•△T=80g×4.18J/(g•℃)×4.0℃=1337.6J,即1.3376KJ,所以实验测得的中和热△H=-
=-53.5 kJ/mol,1.3376KJ 0.025mol
故答案为:-53.5kJ/mol;
③①室温低于10℃时进行实验,散失热量,实验结果的数值偏小,故①正确;
②在量取NaOH溶液的体积时仰视读数,溶液的质量偏大,实验结果的数值偏小,故②正确;
③分多次把NaOH溶液倒入盛有硫酸的小烧杯中,散失热量,实验结果的数值偏小,故③正确;
④实验时用环形铜丝搅拌棒代替环形玻璃搅拌棒,散失热量,实验结果的数值偏小,故④正确;
故选:①②③④;
(3)A.实验时的温度应为酸碱未混合之前的温度,则不是环境温度,故A错误;
B.发生中和反应,溶液温度升高,表明化学能可以转化为热能,故B正确;
C.恰好反应时参加反应的硫酸溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,
恰好反应时氢氧化钠溶液中溶质的物质的量是n.
H2SO4 +2NaOH=Na2SO4+2H 2O
1 2
0.4mol/L×0.03L n
则n=0.4mol/L×0.03L×2=0.024mol,所以浓度是
=1.2mol/L,故C正确;0.024mol 0.02L
D.只是该反应放热,其他有水生成的反应不一定,如氯化铵和氢氧化钡晶体的反应,所以D错误.
故选BC.