问题
选择题
下列叙述正确的是
A.将5.85 g NaCl晶体溶入100 mL水中,制得0.10 mol/L的NaCl溶液
B.将25 g无水CuSO4溶于水制成100 mL溶液,其浓度为1 mol/L
C.将w g a%的NaCl溶液蒸发掉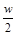 g水,可得到2a%的NaCl溶液(
g水,可得到2a%的NaCl溶液(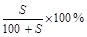 >2a%)
>2a%)
D.将1体积c1mol/L的硫酸用水稀释为5体积,所得稀溶液的浓度为0.2c1mol/L
答案
:CD
题目分析:A.应将5.85 g NaCl晶体溶入水中配制成100ml,制得0.10 mol/L的NaCl溶液;
B. 25 g无水CuSO4物质的量约为0.16mol溶于水制成100 mL溶液,其浓度大于1 mol/L;
C溶液蒸发一半质量,溶液浓度增大一倍。所以正确。
D可根据溶液稀释公式计算,正确。
点评:掌握有关物质的量浓度相关计算。
