问题
计算题
(4分)现有50mL密度为1.18g/mL、质量分数为36.5%的浓盐酸:求
(1)此浓盐酸的物质的量浓度为_________
(2)将此浓盐酸用蒸馏水稀释至200mL,则稀释后溶液中Cl-的物质的量浓度与______ mol/L的氯化镁溶液中的Cl-浓度相同。
答案
(1)11.8mol/L;(2)1.475
题目分析:(1)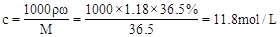
(2)稀释后c(Cl-)= 。一个MgCl2中有2个Cl-,所以与该盐酸中Cl-的物质的量浓度相等的MgCl2的浓度为1.475 mol/L。
。一个MgCl2中有2个Cl-,所以与该盐酸中Cl-的物质的量浓度相等的MgCl2的浓度为1.475 mol/L。
点评:本题基础简单,主要根据两种浓度的转换公式和稀释公式来计算。
