实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH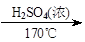 CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚;浓硫酸把乙醇氧化为CO2等。
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
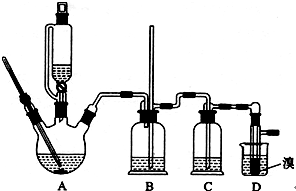
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/oC | 78.5 | 132 | 34.6 |
| 熔点/oC | -130 | 9 | -116 |
(1)A装置上方使用滴液漏斗的优点是:_________________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_____________________(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)B装置的作用是_____________________________________。
(3)在装置C中应加入________(填正确选项前的字母),其目的是______________。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是____________________________.
(5)D装置具支试管内若用溴水代替液溴(假定产物相同),分析其优点________________。
(6)反应过程中应用冷水冷却装置D,其主要目的是_____________;但又不能过度冷却(如用冰水),其原因是_________________________。
(1)便于漏斗内的液体是顺利滴下(1分);B(1分)
(2)平衡压强,检测装置是否发生堵塞(1分)
(3)c(1分);吸收反应生成的SO2等酸性气体(1分)
(4)溴的颜色完全褪去(1分)
(5)产物1,2-二溴乙烷和水不互,溶分层,水在上层起着液封,防止产品挥发的作用(2分)
(6)乙烯和溴单质反应放出热量,冷却可以避免溴的大量挥发(1分);1,2-二溴乙烷的熔点为9℃,过度冷却会变成固体而使进气导管堵塞(2分)
题目分析:(1)A装置上方使用滴液漏斗的优点是便于漏斗内的液体是顺利滴下;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是冷却后补加。
(2)B装置的作用是平衡压强,检测装置是否发生堵塞。
(3)在装置C中应加入氢氧化钠溶液,其目的是吸收反应生成的SO2等酸性气体,因为SO2能被溴氧化。
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去。
(5)D装置具支试管内若用溴水代替液溴(假定产物相同),产物1,2-二溴乙烷和水不互,溶分层,水在上层起着液封,防止产品挥发的作用。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯和溴单质反应放出热量,冷却可以避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的熔点为9℃,过度冷却会变成固体而使进气导管堵塞。
