问题
选择题
200 ml Fe2(SO4)3溶液中含Fe3+ 56g,溶液中SO42—的物质的量浓度是( )
A.5mol/L
B.7.5 mol/L
C.10 mol/L
D.2.5 mol/L
答案
答案:B
题目分析:n(Fe3+)=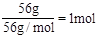 ,c(Fe3+)=
,c(Fe3+)=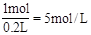 ,则c(SO42-)=7.5mol/L。答案选B。
,则c(SO42-)=7.5mol/L。答案选B。
点评:本题比较基础简单。
200 ml Fe2(SO4)3溶液中含Fe3+ 56g,溶液中SO42—的物质的量浓度是( )
A.5mol/L
B.7.5 mol/L
C.10 mol/L
D.2.5 mol/L
答案:B
题目分析:n(Fe3+)=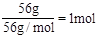 ,c(Fe3+)=
,c(Fe3+)=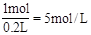 ,则c(SO42-)=7.5mol/L。答案选B。
,则c(SO42-)=7.5mol/L。答案选B。
点评:本题比较基础简单。
化学实验室开放日,小池和小航同学在药品柜中发现一瓶淡黄色粉末,瓶外贴有“过氧化钠(Na2O2)”的标签,这种外观与硫黄相似的物质到底有哪些性质?他们十分好奇,为了弄清它的有关性质,在老师的指导下,他们进行了以下探究活动:
[查阅资料]过氧化钠(Na2O2)在常温下能与水反应生成氢氧化钠和氧气.氢氧化钠能使无色酚酞试液变红色。
[设计实验]过氧化钠与水反应
[进行实验]
| 实验步骤 | 实验现象 | 结论 |
| 1.在试管中加入适量过氧化钠,再加入足量水; | 1.黄色粉末溶解,有 产生 | 产物 (填“有”或“没有”)氧气; |
| 2.用 伸入试管 | 2.木条复燃 | |
| ③再向试管中加入几滴酚酞试液. | 产物有氢氧化钠 |