问题
填空题
(4分)硫酸和硝酸是中学阶段常见的两种强酸,请就两者与金属铜的反应情况回答下列问题:
(1)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 (填写代号):
A.7.32L
B.6.72L
C.20.16L
D.30.24L(2)若使上述反应中剩余的铜片继续溶解,可将溶液稀释并向其中加入硝酸钠,写出反应的离子方程式 。
答案
(共4分)(1)AB (2)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
题目分析:(1)浓硫酸中溶质的物质的量是1.8mol,浓硫酸和铜反应的化学方程式是
Cu+2H2SO4(浓)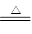 CuSO4+SO2↑+2H2O,所以理论上应该生成SO2的物质的量是0.9mol,标准状况下的体积是20.16L。但由于在反应过程中,浓硫酸的浓度会逐渐降低,所以实际生成的SO2气体的体积小于20.16L,所以答案选AB。
CuSO4+SO2↑+2H2O,所以理论上应该生成SO2的物质的量是0.9mol,标准状况下的体积是20.16L。但由于在反应过程中,浓硫酸的浓度会逐渐降低,所以实际生成的SO2气体的体积小于20.16L,所以答案选AB。
(2)在酸性条件下,硝酸钠具有氧化性,可以继续氧化单质铜,反应的离子方程式是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
点评:该题属于基础性试题,难度不大。关键是理解随着反应的进行浓硫酸的浓度降低这一客观事实。与之相类似的还有二氧化锰和浓盐酸的反应等。
