(1)硬脂酸甘油酯皂化反应方程式为______,欲分离出硬脂酸钠,应采用的方法是:①用滤纸过滤②用分液漏斗分液③加热蒸发④加入热的饱和食盐水______
A.④③;B.④②;C.①③;D.④①
(2)在某体积为2L的密闭容器中充入0.5molNO2和1molCO,在一定条件下发生反应:NO2+CO⇌CO2+NO,下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是______
A.容器内气体的密度保持不变
B.NO2的物质的量浓度不再改变
C.容器内气体的平均相对分子质量不变
D.NO2的消耗速率与CO2的消耗速率相等
E.容器内气体的总物质的量保持不变.
(1)硬脂酸甘油酯与氢氧化钠反应生成C17H35COONa与甘油: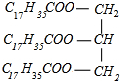 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+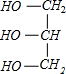 ;向混合液中加入食盐使高级脂肪酸钠的溶解度降低而析出,然后过滤即可,故答案为:
;向混合液中加入食盐使高级脂肪酸钠的溶解度降低而析出,然后过滤即可,故答案为: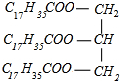 +3NaOH→3C17H35COONa+
+3NaOH→3C17H35COONa+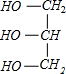 ;D;
;D;
(2)A.容器内的气体反应前后遵循质量守恒,容器内气体的质量保持不变,密度不变,不一定是平衡状态,故A错误;
B.NO2的物质的量浓度不再改变是平衡状态,故B正确;
C.容器内气体的平均相对分子质量在数值上=
,始终是一个不变量,所以容器内气体的平均相对分子质量不变时,不一定是平衡状态,故C错误;m n
D.NO2的消耗速率与CO2的消耗速率相等,说明正逆反应速率相等,是平衡状态,故D正确;
E.反应是一个前后体积不变的反应,容器内气体的物质的量保持不变,不一定是平衡状态,故E错误.
故答案为:BD.