某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案:请回答以下问题:
(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有______;
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净:______;
(3)评价步骤②的操作中难以控制之处______,请你提出一个合理而比较容易操作的实验方案(药品可任选)______,该反应的分子方程式为:______;
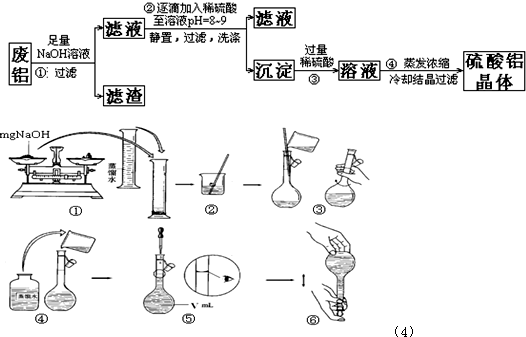
(4)步骤①中使用的NaOH溶液以4mol/L为宜.某同学称量mgNaOH固体配制V m L 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中错误的是(填操作序号)______.
(1)过滤实验用到的玻璃仪器有:烧杯、漏斗、玻璃棒,
故答案为:烧杯、漏斗、玻璃棒;
(2)洗涤沉淀不干净时,在沉淀表面会附着硫酸钠,硫酸根的检验方法:取最后一次洗涤液,加入几滴BaCl2溶液,若无白色沉淀生成则洗涤干净,
故答案为:取最后一次洗涤液,加入几滴BaCl2溶液,若无白色沉淀生成则洗涤干净;
(3)偏铝酸钠和少量的酸反应会生成氢氧化铝沉淀,酸稍过量,沉淀会溶解,但是让溶液的pH=8~9难以控制,可以向偏铝酸钠中通入过量CO2气体来制取氢氧化铝,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)①氢氧化钠易潮解,应在小烧杯中称量,故①错误;④在移液时,要用玻璃棒来引流,故④错误;⑤定容时视线要和刻度线相平,不能俯视和仰视,故⑤错误,
故答案为:①④⑤.
